经济合作与发展组织(OECD)成立于1961年,目前已有38个成员国。为规范实验管理,增强实验的有效性和可靠性,确保向登记部门提交的安全性评价数据的可靠性,主要针对农药、医药、化妆品、工业化学品等领域的非临床人类健康和环境安全测试,OECD组织制定了GLP良好实验室规范。
OECD-GLP数据互认体系
OECD-GLP数据互认体系 (MAD,Mutual Acceptance of Data)是指OECD成员国和加入MAD体系的非OECD成员国按照OECD指南和《OECD良好实验室操作规范》获得的化学品实验数据应被其他成员国和加入MAD体系的其他非成员国接受。MAD临时履约国和完全履约国享受的权力有些微差异,具体可参看图1。MAD体系的建立减少了不必要的重复实验,降低企业成本,保护动物福利,避免非关税贸易壁垒,提高经济效益。据统计,目前通过资料互认减少重复试验,OECD MAD系统为OECD成员国、非成员完全加入国和化学品生产商每年节省3.09亿欧元的费用。
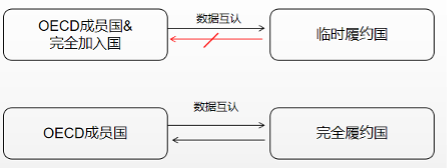
图 1 临时履约国和完全履约国的数据互认差异
由于资料互认具有互惠互利的优越性,非OECD 成员国家要求加入MAD体系的兴趣日益增大,我国于2009 年正式启动申请加入MAD 体系的工作,经过焦灼的沟通谈判,OECD MAD互认有望从农药板块先入手,争取互认。
由于实行MAD数据互认的前提是测试数据必须产生于符合OECD 的GLP 准则要求的实验室,目前OECD 的GLP 准则已在世界范围内得到广泛承认和实施。以下简单介绍下美国和德国的农药GLP体系
1)美国:
美国EPA GLP是一套联邦政府可强制执行的法规,而OECD-GLP是指导性文件,不具有法律效益。美国农药GLP执行40CFR法规第160部分,工业化学品GLP执行40CFR法规第792部分。EPA GLP受到法律的约束和管控,因此与其他国家的GLP认证不同,EPA GLP框架下不要求发放实验室合规证书。此外EPA GLP法规要求实验室对每项研究的GLP合规性声明进行自行验证,如果发现该声明不实,EPA可采取法律行动。
美国GLP检查分为现场机构检查和数据核查两部分,其中现场机构检查主要是审查机构是否符合GLP法规要求,数据核查主要是审查试验的科学性和完整性、是否按照标准操作规程进行以及原始数据是否支持最终报告等,GLP检查程序与OECD GLP基本一致。美国大约有1200家实验室接受GLP审查,提交给EPA接受部门的一部分农药研究每年接受核查。一般从未接受过检查的实验室、过往合规性检查情况很差的实验室以及每年提交报告过多的实验室会受到EPA相关部门的重点审查。
2)德国:
德国GLP框架主要通过一些法规指令、指南和相关主题的欧盟法规进行,如2004/10/EC等。《德国化学品法》(ChemG) 包含了所需非临床安全性研究的GLP合规的约束性条款,是整个安全性实验过程中都必须遵循的GLP法规。德国1990年开始实施ChemG GLP法规,目前已经更新至2020版。德国的GLP法规是强制性的,对于每一项试验,报告持有人都需要提交试验的GLP证书和GLP合规性声明,以向德国监管机构证明其符合GLP法规要求。
德国GLP申请流程主要分为2个部分,一部分是企业根据欧盟指令2004/9/EEC制定计划并进行预检查,按照Chem-VwV-GLP开展试验审查;;另一部分则是德国主管机构按照相关法规审查申请程序和文件,满足要求的实验室则会纳入GLP合规性监管项目,并会定期进行核查。试验机构必须在3年内进行重新申请才能继续保留在GLP监管项目中。
德国目前有151个试验机构,相关GLP文件、试验机构清单等信息,均可在德国GLP联邦管理局网站上进行查找:https://www.bfr.bund.de/en/glp_federal_bureau-1488.html
中国GLP体系,以及与OECD-GLP体系的异同分析
我国于1993年开始建立中国GLP管理法规,2006年农业部颁布了《农药良好实验室考核管理办法》,为推动我国加入OECD/GLP数据互认协议迈出了重要一步。2008 年开始对农药测试实验室进行GLP 检查和考核,2010 年5 月公布了6 个农药检测GLP 实验室。2017年农业部颁布了《农药登记试验单位评审规则》、《农药登记试验质量管理规范》等,规定了GLP认定范围、认定程序以及实验室的职责要求等。中国农药登记实验单位认定作为一项行政许可,认定范围包括产品化学、药效试验、毒理学试验、残留试验和环境影响试验。截止到目前,农业农村部批准了177家试验单位,其中产品化学38家,药效93家,残留63家,毒理学18家,环境影响27家。中国农药GLP认定有效期为5年。
我国是非OECD成员国,非成员国加入MAD体系必须建立GLP执行和监督体系。我国农药GLP体系主要遵循《农药登记试验管理规范》等一系列准则,整体内容基本与OECD-GLP准则一致,尤其是实验质量保证、SOP、实验设施等,但在GLP实验认定范围和认定年限上存在一定差异,OECD的农药GLP试验范围主要涉及人类健康和环境安全试验,与OECD-GLP不同的是我国也将药效试验纳入GLP认定范围,据了解,目前OECD也正在尝试将卫生杀虫剂药效纳入OECD-GLP认定范围中。OECD-GLP认定时需要申请者缴纳评审费用,且认定有效期一般只有2~3年,而我国实验单位申请农药GLP资质认定时不需要缴纳费用,且GLP认定有效期为5年(见表1)。
表1 中国与OECD-GLP体系异同
|
|
相同点 |
不同点 |
||||
|
|
审查要素 |
检查流程 |
遵循准则 |
认定范围 |
认定年限 |
费用 |
|
中国 |
组织和人员、质量保证、试验设施、仪器、材料和试剂、试验体系、试验样品、SOP、试验项目实施、最终报告、档案管理 |
资料审查、现场检查、整改审查、综合评审 |
《农药登记试验管理规范》基本遵循OECD-GLP准则 |
产品化学、毒理学、残留、环境影响、药效 |
5年 |
政府出资 |
|
OECD |
理化性质、毒理学、环境毒性、环境行为、残留、分析化学和临床化学试验、其他 |
2-3年 |
申请者承担 |
|||
实现数据互认的前提条件不仅需要遵守OECD GLP规范也需要采用OECD试验导则。我国农药登记试验方法主要分为行业标准和国家标准两类,根据《农药登记资料要求》,目前农药产品化学实验方法有41项,药效实验方法有310项,毒理学试验方法有45项,残留和环境试验方法分别有6项和48项。由于OECD GLP不包含药效范围,因此除药效和中国特有生物试验外,中国农药登记试验其他大部分测试导则均采用OECD方法。
表2 中国对OECD测试导则的采纳情况
|
测试方法 |
中国 |
OECD |
中国采纳OECD |
|
产品化学(理化) |
38 |
23 |
16 |
|
健康影响 |
39 |
79 |
35 |
|
环境影响 |
27 |
39 |
23(2)2 |
|
环境行为 |
12 |
22 |
10(2)3 |
|
残留代谢 |
6 |
9 |
6 |
|
合计 |
1221 |
172 |
90 |
注1:不包含生物农药和全组分分析方法;
注2:包含2个OECD 指南文件;
注3:包括1个OECD 指南文件
总体而言,中国农药中有70%以上的试验方法已经采用OECD方法,也有部分参考ASTM和CIPAC方法,中国试验导则绝大部分已经与国际通用导则接轨,但也有部分试验方法与OECD方法有差异。为更快实现加入数据互认体系,中国方法需与OECD方法协调统一,尤其是毒理试验需要采用最新的OECD方法。此外,由于中国本土特有的生物、土壤体系不同,部分环境影响和残留试验与OECD测试方法存在差异。中国应当按照OECD准则要求,完善测试方法,为实现MAD做好技术支持。







 化学品
化学品
 食品接触材料
食品接触材料
 化妆品
化妆品
 绿色双碳
绿色双碳
 境外农药登记
境外农药登记
 中国农药登记
中国农药登记